胰腺癌患者的希望之光!Daraxonrasib 迈入临床试验终期阶段

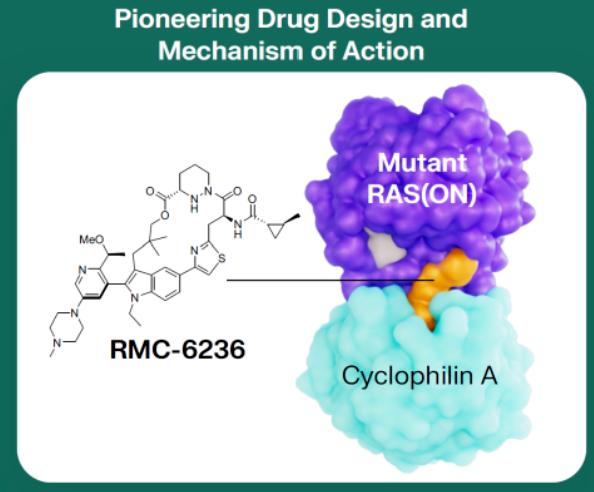
靶点:针对常见的RAS突变,包括G12X、G13X和Q61X,这些突变是胰腺导管腺癌(PDAC)、非小细胞肺癌(NSCLC)和结直肠癌(CRC)等主要癌症的驱动因素。
作用方式:通过阻断RAS(ON)与其下游效应因子的相互作用来抑制RAS信号传导。
最新公布的临床结果 (1L/2L单药以及联合治疗)
01. Daraxonrasib单药治疗:二线转移性胰腺导管腺癌(PDAC)的长期随访(数据截至20250630)
首先,在安全性方面,在83名RAS突变PDAC患者中,daraxonrasib 300毫克每日一次(QD)耐受性良好,其安全性与先前报告的数据一致,未发现新的安全信号。
其次,在疗效方面:daraxonrasib 300毫克每日一次(QD)的治疗剂量在二线(2L)RAS突变PDAC患者中显示出令人信服的抗肿瘤活性和持久性。
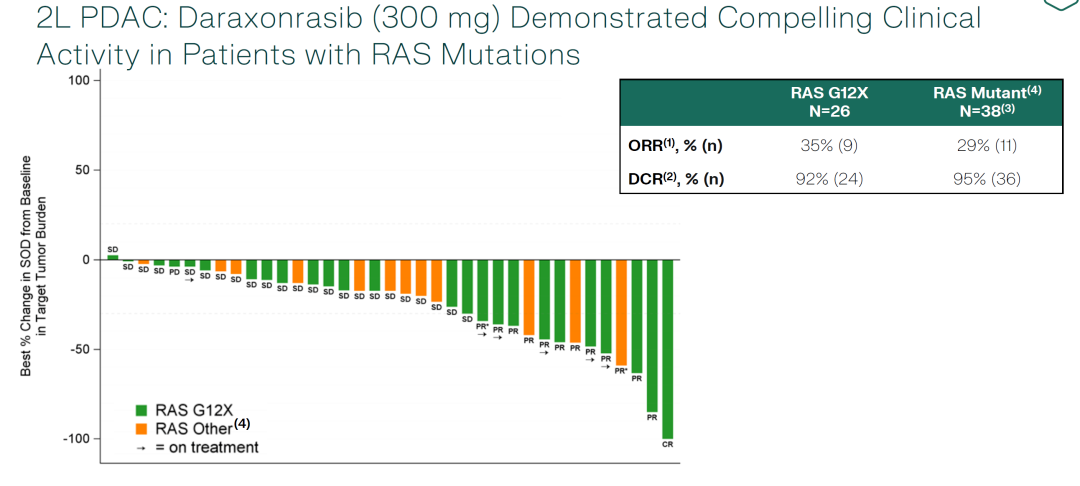
在RAS G12X突变患者(n=26)和任何RAS突变患者(n=38)中观察到的研究结果显示:
确认的客观反应率(ORR)分别为35%和29%。与I期临床结果相似(36%和27%)
疾病控制率(DCR)分别为92%和95%。
中位无进展生存期(PFS)分别为8.5个月和8.1个月。
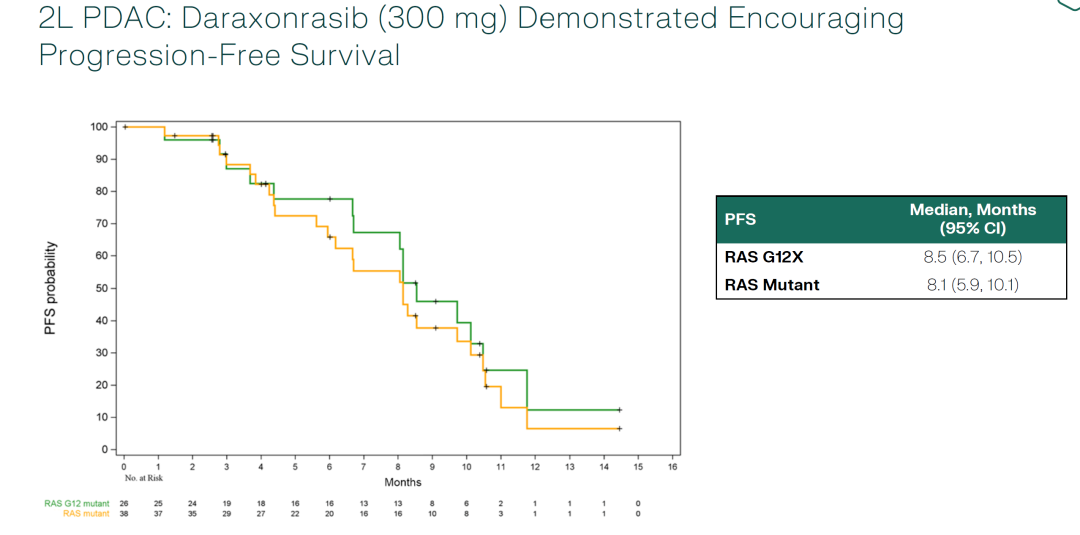
中位总生存期(OS)分别为13.1个月和15.6个月。
中位随访时间为16.7个月。
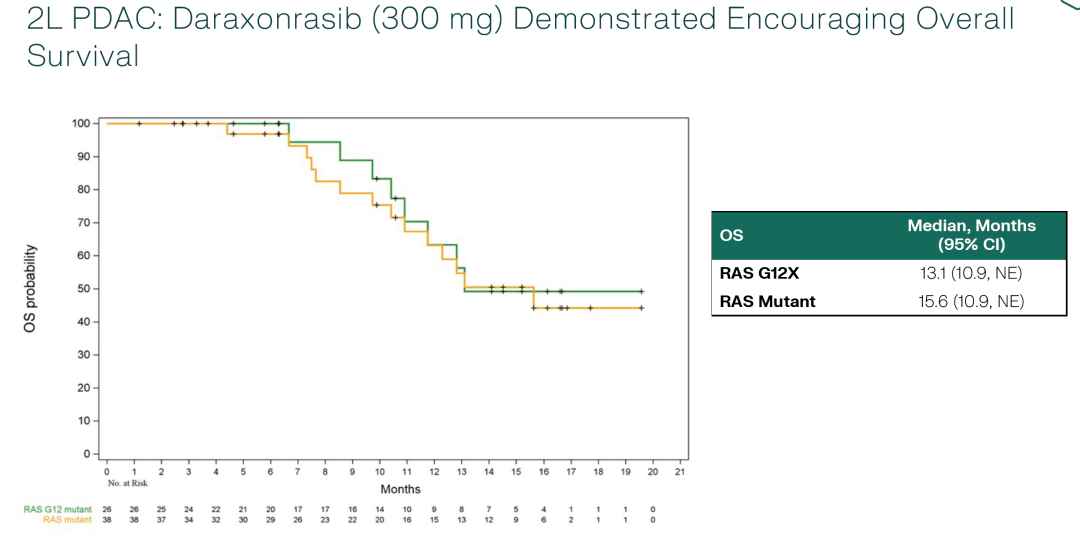
该数据来源于正在进行的3期注册试验RASolute 302,旨在评估daraxonrasib单药治疗作为二线治疗转移性PDAC的疗效,预计在2026年获得预期数据。
02. 在一线转移性胰腺导管腺癌(PDAC)中daraxonrasib单药治疗(数据截至0250728)

客观缓解率(ORR)为47% 疾病控制率(DCR)为89% 中位随访时间为9.3个月。
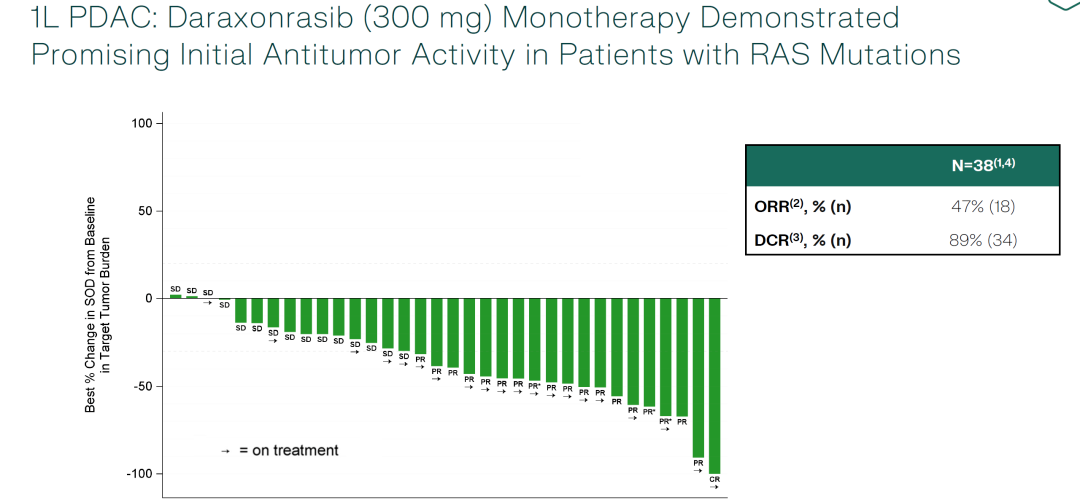
03. Daraxonrasib联合GnP(吉西他滨和白蛋白结合型紫杉醇)在一线转移性胰腺导管腺癌(PDAC)中的应用(数据截至0250728)
Daraxonrasib 与 GnP 联合治疗在胰腺导管腺癌(PDAC)中的临床前研究结果显示:
Daraxonrasib 单药在胰腺癌细胞系(如 Capan-1,携带 KRAS G12V 突变)能够显著抑制肿瘤生长,但效果有限,而联合了 GnP 显著增强了抗肿瘤效果,肿瘤生长抑制更为明显,且效果更为持久。
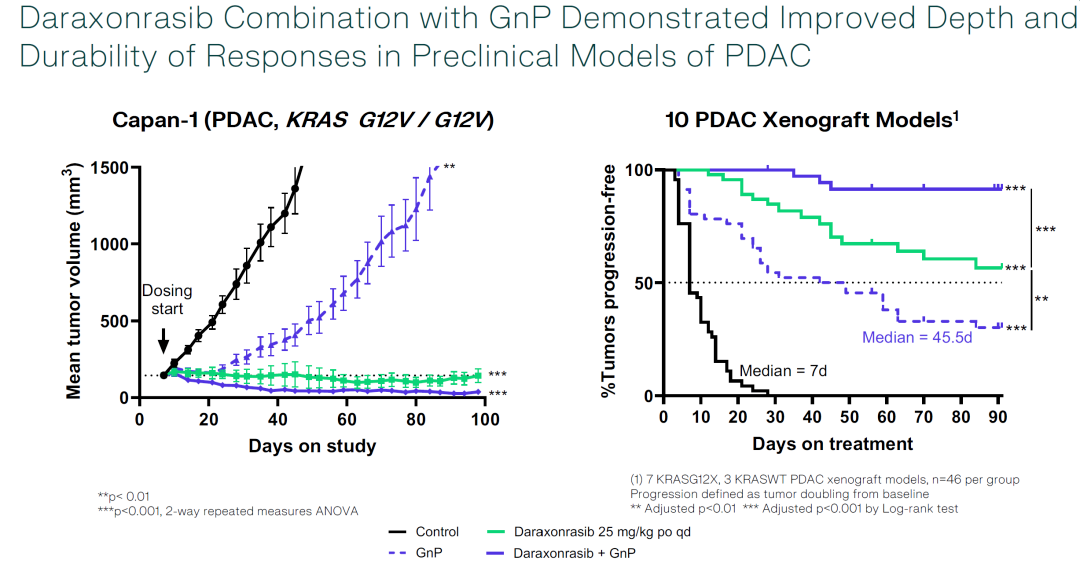
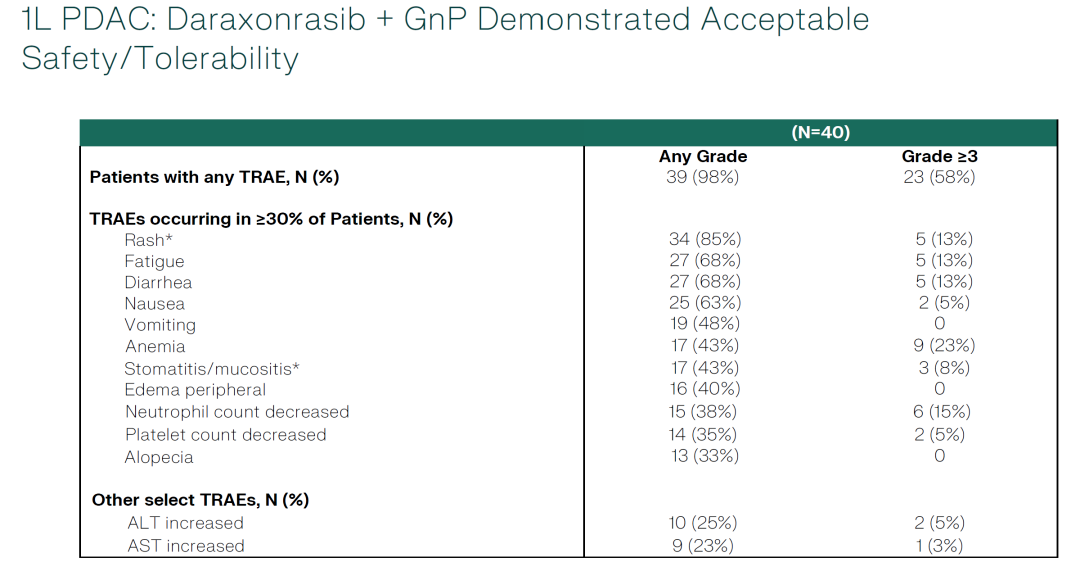
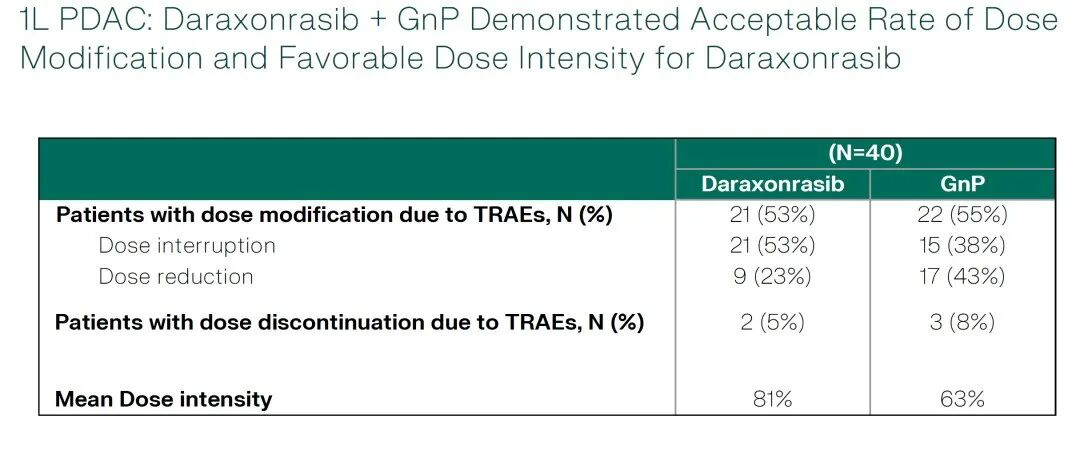
客观缓解率(ORR)为55% 疾病控制率(DCR)为90% 中位随访时间为6.9个月。 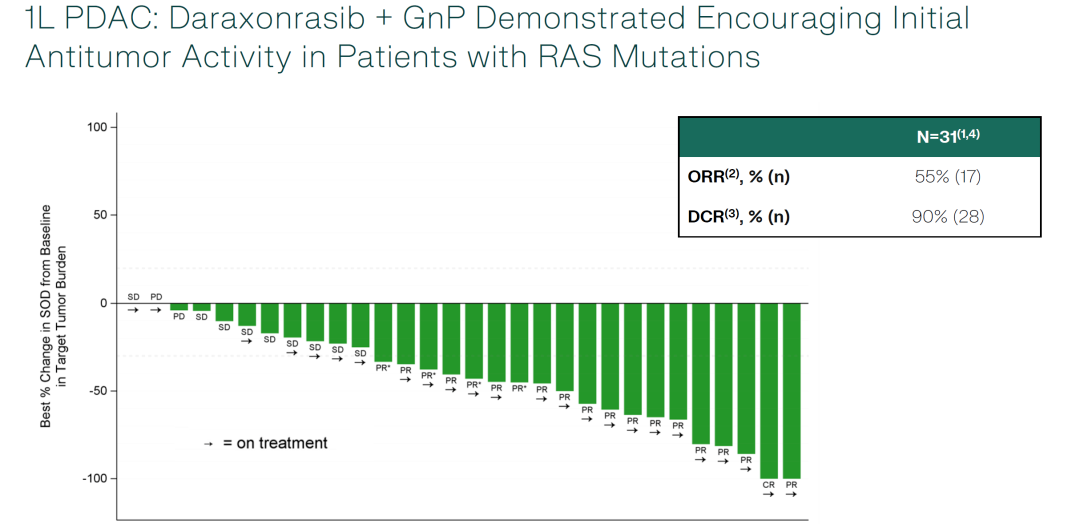
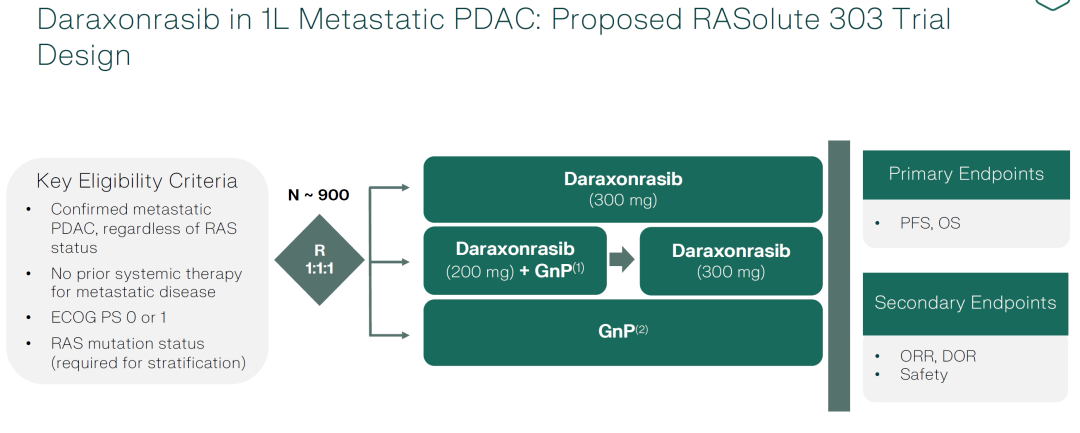
关于RASolute 303
RASolute 303 是 一项全球性、随机、三臂的 3 期注册临床试验,旨在评估 daraxonrasib 单药治疗以及 daraxonrasib 联合吉西他滨和白蛋白结合型紫杉醇(GnP)在一线转移性胰腺导管腺癌(PDAC)患者中的疗效和安全性。
研究目标:
主要目标:评估 daraxonrasib 单药治疗和 daraxonrasib 联合 GnP 治疗在一线转移性 PDAC 患者中的疗效和安全性,与标准治疗(GnP)进行比较。
次要目标:评估客观缓解率(ORR)、反应持续时间(DOR)、疾病控制率(DCR)和安全性。
研究设计:
三臂随机对照试验:
Daraxonrasib 单药治疗组:每日口服 daraxonrasib 300 mg。
Daraxonrasib 联合 GnP 治疗组:每日口服 daraxonrasib 200 mg,联合标准剂量的 GnP,在 28 天周期的第 1 天和第 15 天给药(RVMD选择200mg而不是300mg,可能考虑到的是平衡联合疗法中药物的疗效与毒性,并且可能是维持daraxonrasib强度的较合适的剂量)。
对照组:标准剂量的 GnP 治疗。
总结
RASolute 302:二线转移性PDAC的全球3期注册试验,预计2025年完成入组,2026年公布数据。
RASolute 303:一线转移性PDAC的全球3期注册试验,计划2025年第四季度启动。
RASolute 304:可切除PDAC的全球3期注册试验,计划2025年第四季度启动。

在胰腺导管腺癌(PDAC)治疗领域,存在重大未满足的医疗需求。Daraxonrasib的作用机制、广泛的RAS突变覆盖范围以及广泛的临床前特征表明,其与PDAC的致癌驱动因素高度匹配。临床数据支持其具有有前景的单药治疗潜力,长期随访数据和一线治疗的初步结果均显示了这一点,联合化疗的初步结果也令人鼓舞。目前,正在进行广泛的、晚期的全球开发计划,旨在将daraxonrasib确立为PDAC治疗的新全球标准。期待该药物早日以优秀的临床结果问世,造福广大患者。





































请先 登录后发表评论 ~